Gel-one
Oplysningerne På Webstedet Er Ikke Medicinsk Rådgivning. Vi Sælger Ikke Noget. Nøjagtigheden Af Oversættelsen Er Ikke Garanteret. Ansvarsfraskrivelse
Resume af lægemiddeloversigt
Hvad er gel-one?
Gel-One (tværbundet hyaluronat) er en injicerbar hyaluronatgel, der er godkendt til behandling af slidgigt (OA) af knæet, der ikke har reageret tilstrækkeligt på ikke-farmakologisk terapi, ikke-steroide antiinflammatoriske lægemidler (NSAID'er) eller væddelæg. Acetaminophen.
Hvad er bivirkninger af gel-one?
Almindelige bivirkninger af gel-one inkluderer:
- Fælles hævelse eller smerte
- Fluidopbygning omkring knæet
- Fælles stivhed
- reaktioner på injektionsstedet (smertevarme rødme blå mærker af kløe)
- artritis og
- Ændringer i gang
Dosering til gel-one
Gel-en hyaluronat pakkes i en enkeltinjektionsdosis 3 ml sprøjte (1% opløsning [10 mg/ml] 30 mg total hyaluronan). Det injiceres i det intraartikulære rum på knæet.
Hvilke stoffer stoffer eller kosttilskud interagerer med gel-one?
Gel-one kan interagere med andre lægemidler. Fortæl din læge alle medicin og kosttilskud, du bruger.
Gel-one under graviditet eller amning
Fortæl din læge, hvis du er gravid eller ammer, før du modtager gel-one.
Yderligere oplysninger
Vores gel-one (tværbundet hyaluronat) bivirkninger lægemiddelcenter giver et omfattende overblik over tilgængelige lægemiddelinformation om de potentielle bivirkninger, når du tager denne medicin.
FDA -lægemiddelinformation
- Lægemiddelbeskrivelse
- Indikationer
- Bivirkninger
- Advarsler
- Overdosis
- Klinisk farmakologi
- Medicin vejledning
Forsigtighed: Forbundsret begrænser denne enhed til salg af eller i størrelsesordenen en læge eller korrekt licenseret praktiserende læge.
Beskrivelse til gel-one
Gel-One® er en steril gennemsigtig og viskoelastisk hydrogel sammensat af tværbundet hyaluronat et derivat af stærkt oprenset natriumhyaluronat (hyaluronan) ekstraheret fra kyllingekam. Hyaluronan er et polysaccharid indeholdende gentagne disaccharidenheder af glukuronsyre og N-acetylglucosamin. I Gel-One®-tråde af hyaluronan er der bundet til hinanden via dimerer af kanelsyre, hvilket resulterer i øget viskoelasticitet.
Anvendelser til gel-one
Gel-One® er indikeret til behandling af smerter i slidgigt (OA) af knæet hos patienter, der ikke har reageret tilstrækkeligt på ikke-farmakologisk terapi ikke-steroide antiinflammatoriske lægemidler (NSAID'er) eller enkle smertestillende midler. Acetaminophen.
Dosering til gel-one
Detaljeret enhedsbeskrivelse
Hver forudfyldt sprøjte med 3 ml gel-one® indeholder:
| Tværbundet hyaluronat | 30,0 mg |
| Natriumchlorid | 24,3 mg |
| Dibasisk natrium | |
| Fosfatdodecahydrat | 0,89 mg |
| Natriumdihydrogen | |
| Fosfatdihydrat | 1,93 mg |
| Vand til injektion | Q.S. til 3 ml |
Hvor leveret
Gel-One® leveres i en 3 ml engangsforpligtet glassprøjte indeholdende 3 ml Gel-One®. Indholdet af sprøjten er sterilt. Produktet er latexfrit.
Opbevaringsinstruktioner
Brug ikke Gel-One®, hvis blisterpakken er åbnet eller beskadiget, eller hvis der er revner eller brud i den forudfyldte sprøjte. Opbevares i den originale pakke under 25 ° C (25 ° C). Frys ikke. Brug ikke efter udløbsdato, der er angivet på pakken.
Brug til brug
Forsigtighed: Sterilt indhold. Den forudfyldte sprøjte er beregnet til engangsbrug. Indholdet af sprøjten skal bruges umiddelbart efter, at emballagen er åbnet. Kasser enhver ubrugt gel-one®.
Advarsel: Brug ikke samtidig desinfektionsmidler, der indeholder kvaternære ammoniumsalte til hudforberedelse, fordi natriumhyaluronan kan udfælde i deres nærvær.
Gel-One® leveres i en engangsudfyldt engangssprøjtning. Denne forudfyldte sprøjte er sammensat af et gummipiston [butylgummi: latexfri] gummitipshætte [Butylgummi: latexfrit] fingergreb og stemplet stang og pakkes i en støbt plastik A-PET-film Blister med en Tyvek®-låg.
Gel-One® er designet til at være en enkelt intraartikulær injektion i knæleddet.
- Streng aseptisk administrationsteknik skal følges.
- Fjern ledstrømning, hvis den er til stede gennem en 18-20 g nål, før du injicerer Gel-One®. Oprethold nålplacering i leddet, mens du kobler tilslutningen af sprøjten, der blev brugt til at lindre ledstrømning. Kasser sprøjten indeholdende den fjernede ledstrømning. Den samme sprøjte bør ikke bruges til både fjernelse af effusion og injektion af gel-one®.
- Skræl blister Tyvek® -låg fra blisterpakken, og fjern sprøjten.
- Fjern spidshætten forsigtigt i sprøjten og fastgør aseptisk sprøjten til en 18-20 g nål. For at sikre en tæt tætning og for at forhindre lækage under administration fastgør nålen tæt, mens den holder Luer -låsen fast. Hvis effusion tidligere blev fjernet, skal du forbinde sprøjten til nålen, der allerede er placeret i leddet. Drej spidshætten, før du trækker den af for at minimere produktlækage.
- Injicer Gel-One® i knæleddet gennem nålen ved hjælp af aseptisk injektionsteknik.
- Injicér den fulde 3,0 ml gel-one® i knæet. Hvis behandlingen administreres til begge knæ, skal du bruge en separat sprøjte af gel-one® for hvert knæ.
- Injektion af subkutan lidocaine eller lignende lokalbedøvelse kan udføres inden injektion af Gel-One®.
- Kasser enhver ubrugt gel-one®.
Corporation 6-1 Makya-kya-kya-kya-koda-koda-koda-koda-koda-koda-kyado 46580 USA 1-800-348-2759 (US); 1-574-372-4 Revideret: maj 2011
Bivirkninger for gel-one
Bivirkninger
Rapporterede enhedsrelaterede bivirkninger
De mest almindelige bivirkninger, der er relateret til Gel-One®-injektion rapporteret i den kliniske undersøgelse, er følgende:
- Fælles hævelse
- Fælles effusion
- Arthralgia
Alle bivirkninger, der er relateret til Gel-One®-injektion rapporteret i den kliniske undersøgelse, findes i resume af bivirkninger.
Potentielle bivirkninger
Følgende bivirkninger er blandt dem, der kan forekomme i forbindelse med intraartikulære injektioner.
- Arthralgia
- Fælles stivhed
- Fælles effusion
- Fælles hævelse
- Fælles varme
- Smerter i injektionsstedet
- Artritis
- Leddyr
- Gangforstyrrelse
I henhold til efter-markedsføringserfaring af andre natriumhyaluronatpræparater er anafylaktiske/ anafylactoidreaktioner ledsaget af kortvarig hypotension (pludseligt fald i blodtryk) sjældent rapporteret over hele verden, som alle løste enten spontant eller efter konservativ behandling.
Lægemiddelinteraktioner for gel-one
Ingen oplysninger leveret.
Advarsler for gel-one
- Brug ikke samtidig desinfektionsmidler, der indeholder kvaternære ammoniumsalte til hudforberedelse, fordi natriumhyaluronat kan udfælde i deres nærvær.
- Injicer ikke Gel-One® intravaskulært.
Forholdsregler for gel-one
Generel
- Streng aseptisk administrationsteknik skal følges.
- Fjern fælles effusion, hvis den er til stede, før du injicerer Gel-One®.
- Sikkerheden og effektiviteten af brugen af gel-one® i andre samlinger end knæet og for andre forhold end slidgigt er ikke blevet fastlagt.
- Sikkerheden og effektiviteten af brugen af Gel-One® samtidig med andre intraartikulære injektionsmidler er ikke etableret.
- Sikkerheden og effektiviteten af en gentagen behandlingscyklus af Gel-One® er ikke blevet fastlagt.
- Brug forsigtighed, når du injicerer Gel-One® i patienter, der er allergiske over for kanel-aviærproteiner fjer og/eller ægprodukter.
- Sikkerheden og effektiviteten af Gel-One® i alvorligt betændte knæleddet er ikke blevet fastlagt.
- Injicer ikke Gel-One® ekstra-artikulært eller i synovialvævet og kapslen.
- Sterilt indhold. Den forudfyldte sprøjte er beregnet til engangsbrug. Indholdet af sprøjten skal bruges umiddelbart efter, at emballagen er åbnet. Kasser enhver ubrugt gel-one®.
- Brug ikke Gel-One®, hvis blisterpakken er åbnet eller beskadiget, eller hvis der er revner eller brud i den forudfyldte sprøjte. Opbevares i den originale pakke under 25 ° C (25 ° C). Frys ikke. Brug ikke efter udløbsdato, der er angivet på pakken.
Brug i specifikke populationer
Graviditet
Sikkerheden og effektiviteten af Gel-One® er ikke blevet etableret hos gravide kvinder.
Sygeplejerske mødre
Det vides ikke, om Gel-One® udskilles i human mælk. Sikkerheden og effektiviteten af Gel-One® er ikke blevet fastlagt hos ammende kvinder.
Pædiatri
Sikkerheden og effektiviteten af Gel-One® er ikke blevet påvist hos pædiatriske patienter ( <21 years of age).
Overdoseringsoplysninger til gel-one
Ingen oplysninger leveret.
Kontraindikationer for gel-one
- Administrer ikke Gel-One® til patienter med kendt overfølsomhed (allergi) over for Gel-One® eller natriumhyaluronatpræparater.
- Injicer ikke Gel-One® i knæene hos patienter, der har hudsygdomme eller infektioner i området med injektionsstedet.
Klinisk farmakologi for Gel-One
Klinisk undersøgelse
Undersøgelsesdesign
Sikkerheden og effektiviteten af en enkelt injektion af Gel-One® til behandling af symptomatisk slidgigt i knæet blev undersøgt i en potentiel randomiseret og dobbeltblind kontrolleret undersøgelse udført ved 25 centre i USA. Sikkerheden og effektiviteten af en enkelt injektion af Gel-One® blev bekræftet ved protokol SI-6606/01.
I alt 379 patienter blev randomiseret med et forhold på 2: 1 mellem Gel-One® (n = 251) til PBS (n = 128); Både efterforskere og patienter blev blændet for behandlingsfordeling. Dataindsamling omfattede patientreporterede Western Ontario- og McMaster-universiteter osteoarthritis (WOMAC) Visual Analog Scale (VAS) score resultatmålinger i rheumatologiske kliniske forsøg og osteoarthritis Research Society International Responsees (Omeract-Oarsi-svar) Læge og patientens globale vurderinger og bivirkninger (AES). Den primære effektivitetsanalyse var en sammenligning efter 13 uger mellem Gel-One® og PBS-behandlingsgrupper af ændringer fra baseline i WOMAC VAS-smertersundersanlæg målt i en 100 mm skala.
Patientpopulation og demografi
Af de 379 tilmeldte patienter modtog 377 patienter enten Gel-One® eller PBS-injektion, og 375 patienter blev analyseret for den hensigt at behandle (ITT) population. Patienter rapporterede smerter med symptomatisk OA af knæet defineret af WOMAC VAS -smertersundersæsen på> 40 mm i undersøgelsens knæ og <20 mm in the contralateral knee. Patients meeting the following criteria were excluded at rogomization; Kellgren-Lawrence Grade 4 severe inflammation or joint effusion in either knee. The ITT population included all treated patients who had any post-injection evaluations. Table 1 summarizes baseline og patient demographic characteristics for the ITT population.
Behandling og evalueringsplan
Efter et indledende screeningsbesøg blev støtteberettigede patienter randomiseret til at modtage enten en enkelt injektion af Gel-One® eller en enkelt injektion af PBS. Patienter i begge behandlingsgrupper modtog en intraartikulær injektion i det identificerede knæled i uge 0. Effektivitet og sikkerhedsforanstaltninger blev vurderet ved opfølgningsbesøg i uger 1 3 6 9 og 13.
Patienter, der brugte NSAID'er i stabile doser over 4 uger før undersøgelsen af injektion, fik lov til at fortsætte med det samme regime. Intermitterende anvendelse af kortvirkende opiater blev tilladt under undersøgelsen. Acetaminophen blev tilvejebragt til patienter som en redningsmedicin op til 4000 mg pr. Dag. Al medicin var forbudt inden for 24 timer før hvert evalueringsbesøg.
Bivirkninger Summary
Blandt Gel-One®-behandlingsgruppen (249 patienter) blev 483 bivirkninger hos 172 patienter (69,1%) rapporteret. Blandt PBS -behandlingsgruppen (128 patienter) blev 216 bivirkninger hos 81 patienter (63,3%) rapporteret. Der var ingen statistisk signifikant forskel i forekomsten af bivirkninger mellem Gel-One® og PBS-behandlingsgrupper. Bivirkninger, der forekom hos mere end 5% af patienterne i begge behandlingsgrupper, omfattede fælles hævelse (knæ) fælles effusion (knæ) arthralgi (knæ eller hofte) og infektioner i øvre luftvej (se tabel 2).
De mest almindelige bivirkninger, der var relateret til Gel-One®-injektion rapporteret i denne undersøgelse, var fælles hævelse (14,1%) fælles effusion (11,2%) og arthralgia (7,6%).
Yderligere bivirkninger relateret til Gel-One®-injektion inkluderede smerter i injektionsstedet (2,0%) ledstivhed (0,8%) muskelsvaghed (0,8%) svimmelhed (0,8%) erythema (0,8%) effusion (0,4%) injektionsstedet Bruising (0,4%) injektionssted ERythema (0,4%) hævelse (0,4%) øgede alaninaminotans (0,4%) injektionsstedet) øget bolig (0,4%) hævelse Celletælling (0,4%) rygsmerter (0,4%) muskelspasmer (0,4%) synovitis (0,4%) spændingshovedpine (0,4%) udslæt (0,4%) udslæt kløe (0,4%) og hypertension (0,4%) (se tabel 3).
Der var hverken alvorlige bivirkninger eller pseudoseptiske reaktioner relateret til Gel-One®-injektion.
Neomycin polymyxin B og dexamethason oftalmisk
Kliniske effektivitetsresultater
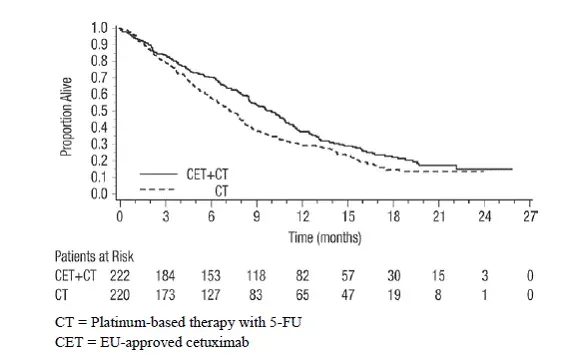
Undersøgelsen af den primære endepoint WOMAC-smerteres underskore i uge 13 demonstrerede, at Gel-One® var bedre end PBS med en 6,39 mm fordel i uge 13 i ITT-befolkningen (P = 0,0374) (se tabel 4 og figur 1).
Resumé af resultaterne af sekundære effektivitet er vist i tabel 5 og 6.
Tabel 1. Patientens baselineegenskaber - ITT -befolkning
| Variabel | Gel-One® (N = 247) | PBS (N = 128) | |
| Alder (år) | Gennemsnit (SD) | 60.9 (10.2) | 60.3 (10.0) |
| Køn (n) | Han | 100 (40,5%) | 51 (39,8%) |
| Kvinde | 147 (59,5%) | 77 (60,2%) | |
| K -l score - Undersøgelse af knæ (n) | 1 | 21 (8,5%) | 18 (14,1%) |
| 2 | 94 (38,1%) | 47 (36,7%) | |
| 3 | 132 (53,4%) | 63 (49,2%) | |
| Undersøg knæ | |||
| WOMAC Pain Subscore (mm) | Gennemsnit (SD) | 70.7 (14.4) | 68.0 (13.1) |
| Total WOMAC -score (mm) | Gennemsnit (SD) | 69.5 (16.0) | 67.8 (14.7) |
| WOMAC fysisk funktion (mm) | Gennemsnit (SD) | 68.9 (17.4) | 67.6 (15.8) |
| WOMAC Stivhed (mm) | Gennemsnit (SD) | 71.6 (17.5) | 69.3 (17.3) |
| Kontralateralt knæ | |||
| WOMAC Pain Subscore (mm) | Gennemsnit (SD) | 7.3 (5.5) | 7.6 (5.6) |
Tabel 2. Bivirkninger, der forekommer hos ≥ 5% af de behandlede patienter
| System Organ Class | Foretrukket udtryk | Gel-One® (N = 249) | PBS (N = 128) |
| Muskuloskeletale og bindevævsforstyrrelser | Fælles hævelse (knee) | 70 (28,1%) | 36 (28,1%) |
| Fælles effusion (knee) | 58 (23,3%) | 33 (25,8%) | |
| Arthralgia (knee/hip) | 44 (17,7%) | 15 (11,7%) | |
| Infektioner og angreb | Infektioner i øvre luftvej | 16 (6,4%) | 6 (4,7%) |
Tabel 3. Bivirkninger relateret til undersøgelsesbehandling
| System Organ Class | Foretrukket udtryk | Gel-One® (N = 249) | PBS (N = 128) |
| Muskuloskeletale og bindevævsforstyrrelser | Fælles hævelse (knee) | 35 (14,1%) | 15 (11,7%) |
| Fælles effusion (knee) | 28 (11,2%) | 13 (10,2%) | |
| Arthralgia (knee/hlp) | 19 (7,6%) | 12 (9,4%) | |
| Fælles stivhed (knee) | 2 (0,8%) | 1 (0,8%) | |
| Muskel svaghed (knæ) | 2 (0,8%) | 1 (0,8%) | |
| Rygsmerter | 1 (0,4%) | 1 (0,8%) | |
| Fælles varme (knee) | 0 | 1 (0,8%) | |
| Muskelspasmer (knæ) | 1 (0,4%) | 0 | |
| Synovitis (knæ) | 1 (0,4%) | 0 | |
| Generel disorders og administration site conditions | Smerter i injektionsstedet | 5 (2,0%) | 1 (0,8%) |
| Effusion | 1 (0,4%) | 1 (0,8%) | |
| Injektionsstedet erythema | 1 (0,4%) | 1 (0,8%) | |
| Injektionsstedet blå mærker | 1 (0,4%) | 0 | |
| Hævelse | 1 (0,4%) | 0 | |
| Hud og subkutane vævsforstyrrelser | Erythema | 2 (0,8%) | 0 |
| Udslæt | 1 (0,4%) | 0 | |
| Udslæt pruritic | 1 (0,4%) | 0 | |
| Nervesystemforstyrrelser | Hovedpine | 0 | 2 (1,6%) |
| Svimmelhed | 2 (0,8%) | 0 | |
| Brændende fornemmelse | 0 | 1 (0,8%) | |
| Spændingshovedpine | 1 (0,4%) | 0 | |
| Undersøgelser | Forøget alaninaminotransferase | 1 (0,4%) | 0 |
| Øget tælling af hvide blodlegemer | 1 (0,4%) | 0 | |
| Vaskulære lidelser | Hypertension | 1 (0,4%) | 0 |
| Øre- og labyrintforstyrrelser | Høring nedsat | 0 | 1 (0,8%) |
| Infektioner og angreb | Cellulitis | 0 | 1 (0,8%) |
| Skadeforgiftning og proceduremæssige komplikationer | Kontusion | 0 | 1 (0,8%) |
Figur 1: Forbedring fra baseline i WOMAC VAS Pain Subscore i uge 13 - ITT -befolkningen
 |
Tabel 4. Womaca Forbedring af vas smerte fra baseline efter 13 uger (ITT -befolkning (n = 375))b
| Vurderet tidspunkt | Model-estimeret fordel (Gel-One®-PBS) | To-sidet lavere 95% konfidensgrænse (MM) | Tosidet p-værdi |
| I uge 13 | 6,39 mm | 0.37 | 0.0374 |
| a Western Ontario- og McMaster Universities osteoarthritis -indeks (WOMAC) er et sæt standardiserede spørgeskemaer, der bruges af sundhedsrofessionelle til at evaluere tilstanden for patienter med slidgigt i knæet og hoften. Womac Pain Scale er 100 mm. b Analysen er baseret på den kvadratiske spline -model ved knude på 6 uger og i uge 13 for det primære slutpunkt. |
Tabel 5: Omeract-Oarsi-svara - ITT -befolkning
| Oddsforholdb | Tosidet lavere 95% konfidensgrænse for oddsforholdetc | Tosidet p-værdid |
| 1.27 | 0.85 | 0.2418 |
| a Et emne blev betragtet som en omeract-oarsi 'responder1, hvis et af de følgende 2 kriterier blev opfyldt: (1) Hans eller hendes rapporterede forbedring fra baseline i WOMAC VAS Pain Subscore eller WOMAC VAS Fysisk funktionsunderkore var mindst 50%, og den absolutte ændring var mindst 20 mm eller (2) Hans eller hendes rapporterede forbedring fra baseline var mindst 20%, og den absolutte ændring var mindst 10 mm for mindst 2 af de følgende 3 mål: (a) Womacvas Pain Subscore (b) WOMAC VAS Fysisk funktionsundersæsen (c) Emne Global Evaluering. b E (log oddsforhold) - 1 2 7 baseret på GEE -modellen (Log oddsforhold) = loge [sandsynlighed (responder)/ sandsynlighed (ikke-responder)] gei-one/ [sandsynlighed (responder)/ sandsynlighed (ikke-responder)] PBS c Når oddsforhold> 1 [sandsynlighed (responder)/ sandsynlighed (ikke-responder) gei-one]> [sandsynlighed (responder)/ sandsynlighed (ikke-responder) PES] og dermed til fordel for gel-one. d Statistisk ikke signifikant |
Tabel 6: Resumé af sekundær effektiviteta Endpoints i uge 13 - ITT -befolkningen
| Effektivitetsforanstaltningerb | Model-estimeret fordel (Gel-One®-PBS) | Tosidet lavere 95% konfidensgrænse (MM) | Tosidet p-værdic |
| Total WOMAC -score | 5,64 mm | -0.20 | 0.0583 |
| WOMAC Stivhed | 4,91 mm | -1.31 | 0.1216 |
| WOMAC fysisk funktion | 5,42 mm | -0.47 | 0.0714 |
| a Baseret på den kvadratiske spline -model i uge 13. b WOMAC -skala er 100 mm. c P-værdi blev ikke justeret for mangfoldighed af sekundære endepunkter. |
Patientinformation til gel-one
- Giv patienter en kopi af patientinformationen inden brug.
- Forbigående smerte hævelse og/eller effusion af det behandlede knæled kan forekomme efter intraartikulær injektion af Gel-One®. Disse begivenheder løses normalt på egen hånd eller med konservativ behandling.
- Som med enhver invasiv fælles procedure anbefales det, at patienten undgår anstrengende aktiviteter (såsom jogging tennis anden aktiv sports tung løft) og langvarige vægtbærende aktiviteter (såsom stående i mere end en time) inden for 48 timer efter den intra-artikulære injektion af Gel-One®.